我们能创造出易于使用的软件来捕捉蛋白质的复杂行为吗?
蛋白质组学是通过质谱技术对蛋白质进行大规模研究。就像指纹可以在没有目击证人的情况下证明某人在现场一样,质谱仪记录的蛋白质指纹以肽或蛋白质片段的形式引入。质谱仪本身不能从它们的肽中识别蛋白质;相反,这种复杂的分析需要高度专业化的软件程序。
蛋白质组学可以监测样本之间蛋白质丰度的变化,比如正常细胞和患病细胞。一种测量细胞蛋白质组在应激反应中的变化的方法被称为等压串联质量标记(IMT)。IMT包括用独特的化学条形码标记样品中的所有蛋白质肽。一个人可以条形码多达六个不同的蛋白质组进行比较。条形码提供了两个主要优点。首先,标记的蛋白质组可以通过质谱仪同时组合和分析。如果样品单独进样,就会引入不必要的技术误差来源。条形码的第二个优点是,其强度是可测量的,并与相应蛋白质的丰度直接相关。因此,IMT数据提供了指纹和定量信息,供下游软件分析。

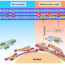
图1所示。蛋白质组学的条形码策略(A- c)和蛋白质组学数据(D)。A,巨噬细胞在体外培养72小时,用干扰素γ (IFN)诱导促炎表型(M1);白细胞介素-4 (IL-)的抗炎表型(M2);或中性表型(无刺激,M0)。B、箭头表示与IMT策略相关的样品收集、蛋白质分离和化学条形码(标签1至6)的多个步骤。C,条形码肽样品汇集并通过质谱仪分析。D,对从三个巨噬细胞实验中获得的蛋白质数据集进行条形码的步骤概述。利用mIMT-visHTS软件对条形码数据集进行合并和分析。
据认为,促炎(M1)巨噬细胞对抗炎(M2)巨噬细胞的优势促进了与动脉粥样硬化和代谢紊乱相关的慢性炎症。我们在体外培养的巨噬细胞中测量了蛋白质组学的变化,以模拟这两种表型。我们还进行了第三次无刺激(M0)实验,作为噪声控制。在三个培养实验中,我们在三天内的六个时间点监测蛋白质组,从而进行了三个IMT 6-plex实验(图1A-C)。
一旦收集到IMT数据,就可以根据相似性对蛋白质行为进行聚类。这一步为每个M1、M2和M0数据集生成15个集群。我们有一项艰巨的任务,从三个数据集中筛选约4000个蛋白质簇,代表约12000个动力学特征。可以想象,由于数据集的规模太大,可能会错过重要的趋势。乍一看,我们发现一些蛋白质在M0、M1和M2中表现相同;其他人在三分之二中表现相似;而另一些则在三种状态下表现出不同的动力学。然而,我们很难以高吞吐量的方式表示这些不同的场景。然后我们意识到,如果我们采取与IMT本身类似的方法,我们的问题可以解决:为每个数据集分配一个条形码,组合数据集,并让软件同时分析它们。我们设想单个输出将促进吞吐量分析(图1D)。

图2所示。仔细看看mIMT-visHTS软件。A,软件根据相似性对蛋白质丰度(动力学)谱进行分组。这些簇代表了在所有三个巨噬细胞数据集中观察到的蛋白质动力学。B,由于数据是条形码的,软件可以很容易地帮助用户探索数据集之间的蛋白质趋势。生物学家可能会问的两个问题被突出显示。问题1涉及在所有三个实验中丰度保持稳定的蛋白质。靶心的单一颜色反映了不受干扰的行为。问题2涉及在M0和M2中丰度保持稳定,但由于促炎转变而受到干扰的蛋白质。彩色靶心表明,113种蛋白质改变了它们的动力学,变成了12个其他簇中的一个。
我们得到的软件工作流,mIMT-visHTS,指的是米ultiplexing各种IMT数据集,然后实现力的可视化图形用户界面h本throughput年代每个靶心代表一种巨噬细胞蛋白行为。靶心颜色越鲜艳,由于培养条件的影响,偏离行为的蛋白质就越多。靶心颜色越少,蛋白质对不同条件的反应就越弱。这些蛋白质的名称可以被提取出来用于后续的研究。因此,visHTS提供了一种简单的方法来评估蛋白质组的各种扰动,这些扰动是成为促炎性或抗炎性巨噬细胞的结果。它作为一个筛选系统运行,不需要理解分析背后复杂的数学运算。
蛋白质组学正变得越来越普遍。因此,数据增长迅速,分析起来也变得更加复杂。visHTS是朝着产生创造性和直观的输出程序的第一步,这是当今生物学家所面临的挑战所必需的。
出版
mIMT-visHTS:一种用于多路等压质量标记数据集的新方法,附带用于蛋白质分析的可视化高通量筛选工具。
Ricchiuto P, Iwata H, Yabusaki K, Yamada I, Pieper B, Sharma A, Aikawa M, Singh SA
蛋白质组学杂志,2015年10月14日












留言回复
你一定是登录发表评论。