肺泡软组织肉瘤的分子靶向治疗
肺泡软组织肉瘤是一种罕见的恶性肿瘤,约占所有软组织肉瘤的1%,通常发生在青少年和青壮年。这种类型的癌症有远处转移和侵袭的倾向,特别是脑和肺。肺泡软部肉瘤(Alveolar soft part sarcoma, asp)的特征是X和17条染色体之间不平衡的非互易易位,t(X;17) (p11.2;q25),导致ASPSCR1-TFE3融合基因。TFE3是肿瘤细胞生长和代谢途径的有效调节剂,包括(mTORC1, c-Met和HIF1α)(图1)。
肿瘤切除是可手术ASPS最有效的治疗干预措施,可导致完全缓解,但如果不能通过手术完全切除肿瘤,预后不良是可以预见的。许多研究表明,化疗药物对ASPS治疗无效,对放疗的反应也存在争议,但靶向治疗似乎是ASPS治疗的一个很好的选择(图2)。
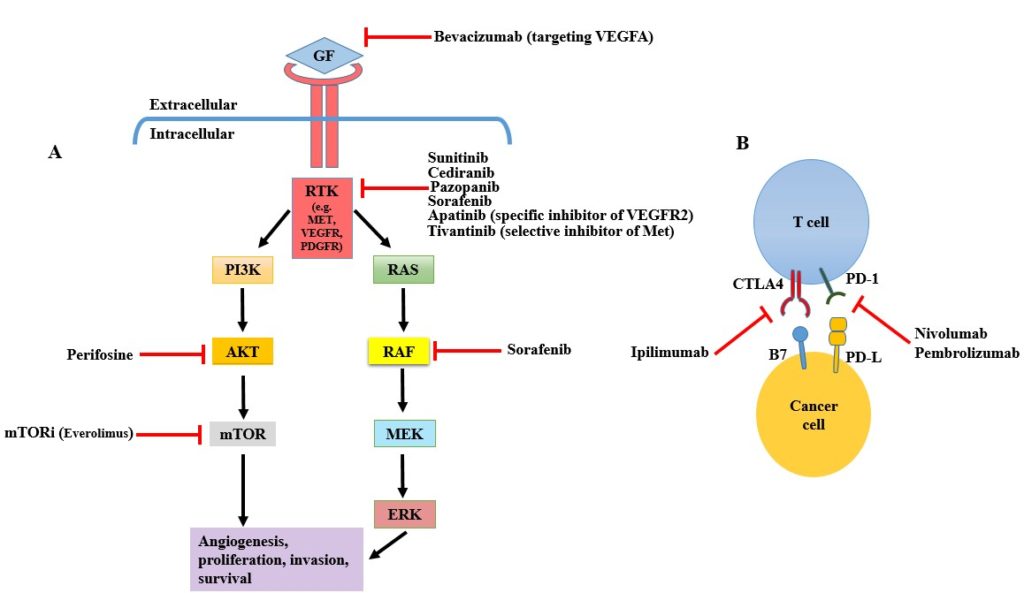
图2所示。ASPS中主要失调的致癌信号通路及其被潜在适用的分子靶向药物抑制的示意图(A)。癌症免疫治疗可能是ASPS治疗的一种挽救性治疗方法(B)。其中一些分子靶向药物,如perifosine, sunitinib, cediranib, pazopanib, everolimus和cabozantinib正在用于ASPS和/或STS治疗的临床试验中。需要更多的研究来更好地评估这些药物治疗ASPS的疗效。(GF:生长因子,RTK:酪氨酸受体激酶,PI3K:磷脂酰肌醇-3激酶,mTOR:雷帕霉素的哺乳动物靶点,MEK:丝裂原活化蛋白激酶,ERK:细胞外信号调节激酶,PD-1:程序性细胞死亡蛋白1,PD-L:程序性死亡配体1,CTLA4:细胞毒性t淋巴细胞相关蛋白4)。
ASPS的转录组学分析显示血管生成和转移靶点如VEGF和c-Met上调,这表明血管生成和转移途径是ASPS的标志,可用于ASPS治疗。肺泡软组织肉瘤是一种高血管肿瘤,因此使用血管生成抑制剂可能是控制ASPS进展的合适选择。联合使用多靶点TKI(酪氨酸激酶抑制剂)和免疫治疗可以改善ASPS患者的预后;然而,需要更多的转化和临床研究来证明这些治疗方法的有效性和安全性。官方manbetx手机版
Mohammad Hasan Soheilifar1,2,拉米赞·阿里·塔赫里1,Reza Zolfaghari Emameh3.,
Abdolvahab Moshtaghian4,哈米德Kooshki1,穆罕默德·雷扎·莫蒂5
1伊朗德黑兰巴基亚塔拉医科大学纳米生物官方manbetx手机版技术研究中心
2官方manbetx手机版伊朗哈马丹医科大学医学院分子医学与遗传学研究中心
3.伊朗德黑兰国家基因工程与生物技术研究所(NIGEB)工业与环境生物技术司能源与环境生物技术部
4塞姆南医科大学研究与官方manbetx手机版技术副主任,塞姆南,伊朗
5马什哈德医学大学医学院伊玛目礼萨医院官方manbetx手机版外科肿瘤研究中心,伊朗马什哈德
出版
肺泡软组织肉瘤的分子景观:分子靶向治疗的意义。
Soheilifar MH, Taheri RA, Zolfaghari Emameh R, Moshtaghian A, Kooshki H, Motie MR
Biomed Pharmacother。2018年7月











留言回复
你一定是登录发表评论。