潜入黏液-聚乙二醇胶束进行口服递送
吞一片扑热息痛治头痛既快又容易。该药物可以在没有任何疼痛或辅助的情况下在所需的时间和地点施用。而像胰岛素这样的生物药物就不是这样了,胰岛素是一种肽激素,会被胃肠道的蛋白水解酶降解,而且缺乏通过肠上皮的运输途径。对于水溶性差的药物,口服给药也有问题,这限制了它们的吸收。尽管现代生物技术和纳米科学的努力,寻找口服途径的疏水和肽/蛋白为基础的治疗仍然是一个长期的挑战。这个问题的性质很复杂。成功的口服给药需要防止低pH值和酶,但必须允许细胞摄取和释放治疗药物。更麻烦的是,肠上皮被一层粘稠的黏液层所覆盖,这层粘稠的黏液层旨在清除体内的外来颗粒,阻止药物运载工具的接近。
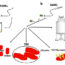
黏液层由称为粘蛋白的糖肽组成。这些大型支链聚合物的网状结构通过纠缠、疏水相互作用和静电相互作用捕获颗粒。解决粘穿透挑战的一种方法是组装能够避免上述相互作用的纳米颗粒。纳米颗粒是利用两亲嵌段共聚物的自组装形成的,其中聚合物链的一部分是亲水的,另一部分是疏水的。在水介质中,疏水尾部倾向于相互面对以避开水环境,导致球形胶束的形成。以聚乙二醇(PEG)为亲水嵌段作为关键元件。这种中性亲水性聚合物为胶束提供了一个“光滑”的电晕,不允许与粘液成分相互作用。此外,胶束的核心由聚(己内酯)或聚(甲基丙烯酸胆固醇)尾部组成,允许装载疏水货物。
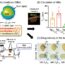
找到一种结构来避免与黏液的相互作用是一回事,而在实践中评估黏液的穿透性是另一回事。使用动物(如大鼠、猪)模型需要时间、金钱和道德考虑。此外,动物模型的复杂性使得量化和比较不同纳米材料之间的结果具有挑战性。在Taipaleenmäki的研究中等在微流体装置中,胶束与充满黏液的通道相互作用,可以观察和记录胶束的渗透行为,从而实现了一种快速简便的黏液渗透评估方法。微流体装置模拟肠道流动,但缺乏上皮本身,包括细胞分泌粘液等特征。肠上皮由四种主要细胞类型组成,但通常使用Caco-2细胞系和HT29-MTX-E12细胞进行模拟。后一种细胞能够分泌粘液。利用共聚焦激光扫描显微镜创建细胞培养物的三维图像,以确认细胞内胶束的位置。
综上所述,基于聚乙二醇的胶束被成功地用于通过黏液层递送模型货物,并且有潜力发展成为口服递送疏水疗法的载体。
林施
奥胡斯大学跨学科纳米科学中心,丹麦奥胡斯
出版
具有聚乙二醇电晕的胶束。
Taipaleenmäki EM, Mouritzen SA, Schattling PS,张勇,Städler B
2017年11月30日












留言回复
你一定是登录发表评论。