微流控肿瘤模型有助于T细胞癌免疫疗法的临床前筛选
癌症免疫疗法利用病人自身的免疫系统来识别和对抗疾病。癌症免疫治疗的一种形式被称为过继性T细胞治疗(ACT),包括分离、基因操作和将能够通过抗原识别靶向肿瘤细胞的工程T细胞重新输注到患者体内。尽管各种方法已被临床批准,并已证明对治疗液体肿瘤(血液肿瘤)如白血病和淋巴瘤有一定的益处,但目前对实体肿瘤的有效治疗非常有限。
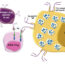
针对实体瘤的T细胞免疫疗法的主要限制之一是肿瘤周围的组织通常被称为肿瘤微环境(TME)。TME是一个由免疫细胞、支持细胞、细胞外基质(ECM)以及抑制T细胞与癌细胞相互作用的淋巴管和血管组成的复杂系统(图1)。事实上,一旦工程T细胞到达肿瘤,它们既需要与癌细胞物理相互作用,摧毁癌细胞,又需要增殖,以维持肿瘤附近大量活跃的T细胞。
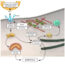
在人体外模拟这些相互作用(体外)以及三维(3D) TME的特性,我们开发了一种微流控装置,该装置由微通道组成,微通道印在一种称为聚二甲基硅氧烷(PDMS)的透明聚合物上,并由玻璃盖盖封闭。微通道中充满了液体或水凝胶。像这样的微流控平台允许(i)多种细胞类型一起在三维ecm样基质中培养;(ii)形成不同化合物和分子的梯度;(iii)细胞相互作用、迁移和粘附的实时可视化;(四)通过改变氧含量来调节微环境。
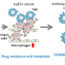
重要的是,在这些三维微流控平台上,已经成功地模拟了每个转移阶段的特定机制(图1),以更好地概括肿瘤进展和肿瘤-免疫系统在TME中的相互作用。此外,工程T细胞的效率已经在这些3D多细胞微流控装置中进行了测试,以筛选不同的工程策略,这些策略与TME中通常发现的生物因素或氧水平的变化相似。
因此,3D微流控肿瘤模型代表了一种有价值的分析方法,可以快速和可重复地测试T细胞对抗实体肿瘤的策略,从而在应用于患者之前微调治疗,从而减轻不必要的临床副作用。T细胞与放疗或化疗的其他协同组合也可以筛选,以确定最佳反应,并为癌症患者提供合理和个性化的治疗。
会Adriani和罗杰·d·卡姆
新加坡-麻省理工学院研究与技术联盟,新加坡官方manbetx手机版
麻省理工学院,剑桥,马萨诸塞州,美国
出版
过继细胞介导的癌症免疫治疗的微流控模型。
阿德里亚尼G,帕维西A,谭AT, Bertoletti A, Thiery JP, Kamm RD
今日毒品发现2016年9月











留言回复
你一定是登录发表评论。