肝脏的恶性循环助长了肥胖糖尿病的流行
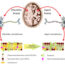
实验性肥胖很容易由饮食中过量的脂肪或碳水化合物产生,并涉及肝脏葡萄糖产生的初始增加和随后血液胰岛素水平的增加,即胰岛素抵抗状态。反过来,升高的血胰岛素刺激肝脏产生脂肪,即“脂质”,这些脂肪首先以非酒精性“脂肪肝”的形式积聚在肝脏中,其次以甘油三酯和胆固醇的形式积聚在血液中,引发心血管问题,最后在脂肪储存库中,特别是腹部,产生典型的“大肚子”。随着脂肪的增加,肝脏产生的其他有害因子增加,肌肉中的葡萄糖代谢受损,胰岛素抵抗恶化。同样的恶性循环也发生在人类身上,如果不加以控制,就会引发成熟型(2型)糖尿病,40岁以上的人中有四分之一患有这种疾病。
 在一系列论文中,坦帕VA医院和南佛罗里达大学的Ro官方manbetx手机版bert Farese博士领导的一个研究小组在实验肥胖模型中表明,胰岛素抵抗严重依赖于一种特殊肝脏蛋白活性的增加,这种酶被称为非典型蛋白激酶C,简称“aPKC”,作为一种“激酶”酶,它将高活性磷酸基团添加到其他蛋白酶上,以改变它们的功能。坦帕研究小组还发现,肝脏中的aPKC酶是“混杂的”,在饮食来源的脂质和胰岛素增加的脂质的双重作用下,aPKC酶被过度激活。不幸的是,饮食导致的肥胖中aPKC的过度激活会导致胰岛素使用的另一种酶的作用和活性降低,这种酶可以减少肝脏产生的葡萄糖。后一种酶被称为蛋白激酶B或“Akt”,众所周知,它通过调节一系列酶来减少肝脏葡萄糖的产生,包括“FoxO1”和“pgc -1 α”,这些酶在肥胖和2型糖尿病人的肝脏中过度活跃。
在一系列论文中,坦帕VA医院和南佛罗里达大学的Ro官方manbetx手机版bert Farese博士领导的一个研究小组在实验肥胖模型中表明,胰岛素抵抗严重依赖于一种特殊肝脏蛋白活性的增加,这种酶被称为非典型蛋白激酶C,简称“aPKC”,作为一种“激酶”酶,它将高活性磷酸基团添加到其他蛋白酶上,以改变它们的功能。坦帕研究小组还发现,肝脏中的aPKC酶是“混杂的”,在饮食来源的脂质和胰岛素增加的脂质的双重作用下,aPKC酶被过度激活。不幸的是,饮食导致的肥胖中aPKC的过度激活会导致胰岛素使用的另一种酶的作用和活性降低,这种酶可以减少肝脏产生的葡萄糖。后一种酶被称为蛋白激酶B或“Akt”,众所周知,它通过调节一系列酶来减少肝脏葡萄糖的产生,包括“FoxO1”和“pgc -1 α”,这些酶在肥胖和2型糖尿病人的肝脏中过度活跃。
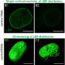
正如最近在哈佛大学期刊《代谢》(Metabolism)上所报道的那样,坦帕研究小组检查了随机从已故的老年被拒绝的人类移植供体中获得的肝脏,发现个体的体重指数(BMI)越高,肝脏中aPKC酶的数量和活性就越高,因此Akt、fox01和PGC-1alpha的变化就越大。产生葡萄糖和脂质的酶增加得越多。事实上,肥胖人群的所有这些肝酶异常都随着体重指数的增加而上升,达到接近2型糖尿病患者的水平。最重要的是,幸运的是,所有2型糖尿病肝细胞中的酶异常都可以通过新开发的靶向并降低aPKC酶活性的药物治疗而逆转。这种对周期中所有异常的广泛纠正是aPKC抑制剂所特有的,而在目前使用的抗糖尿病药物中未见。
除了在分离的肝细胞中使用外,坦帕研究小组还使用aPKC的化学抑制剂来治疗几种伴有肥胖和早期2型糖尿病的胰岛素抵抗小鼠模型。与分离肝细胞的发现一致,最有希望的aPKC抑制剂,当在肥胖糖尿病小鼠中使用时,选择性地抑制肝脏中的aPKC,并在很大程度上逆转所有肝酶异常,从而纠正或预防肥胖的发展,肝脏和血液中的脂质积累,以及血糖水平的升高。虽然这种aPKC抑制剂在2-3个月的小鼠研究中没有出现不良反应,但希望它或目前正在开发的其他化学相关aPKC抑制剂在未来更长期的研究中继续是安全的,并最终被证明是有用的,直接或间接地作为模型,用于治疗人类肥胖和2型糖尿病。
出版
肥胖和2型糖尿病患者肝脏中通过IRS-1、Akt、fox01和PGC-1α表达的非典型pkc依赖性胰岛素信号异常的bmi相关进展
Sajan MP, Ivey RA 3rd, Farese RV
2015年11月










留言回复
你一定是登录发表评论。