慢性淋巴细胞白血病(CLL)的诊断在培养细胞中优于天然细胞
癌症是与年龄有关的疾病。在西方国家,人们的预期寿命比100年前更长,这意味着目前有1-2%的人在他们的一生中面临白血病的诊断。白血病也被称为“血癌”,起源于异常的骨髓细胞。
与人体其他细胞相比,癌细胞确实是“不正常的”:它们具有不同的形状、特性和行为,例如在生长速度方面。众所周知,所有这些“异常特性”都源于肿瘤细胞的“异常遗传”。而“异常基因”因肿瘤类型而异(例如,特定的白血病与乳腺肿瘤相比)。即使在相同的肿瘤实体中,也可以根据其遗传特性定义具有不同临床结果的亚类。因此,利用特定的分子遗传学方法对癌细胞进行研究是癌症诊断的一个重要步骤。

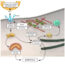
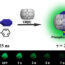
图1所示。A)通过荧光原位杂交(FISH)检测两名慢性淋巴细胞白血病(CLL)患者间期细胞核的遗传改变。第一列显示两个间期细胞核,蓝色(= DAPI)反染,两个红色和两个绿色信号,表明结果正常,P53和ATM基因未缺失。在第二列中,细胞核再次显示出两个绿色信号,但只有一个红色信号,即发现了atm基因的缺失。可见,良好的fish信号既可以在天然材料中获得,也可以在人工材料中获得。
B)通过对60例CLL病例的比较研究发现,培养CLL细胞中如图A所示的这种缺失的检出率比天然CLL细胞高8%以上。
在西方国家,最常见的高龄白血病类型是慢性淋巴细胞白血病(CLL)。CLL是一种异质性获得性疾病。首次确诊的平均年龄在70岁左右;在诊断时,病人可能已经有问题好几年了,因为症状大多不明确。CLL患者可因无痛肿大的淋巴结、盗汗、疲劳、发热、体重减轻、频繁感染和/或左上腹部疼痛以及脾脏肿大而出现MD。一般来说,CLL的进展非常缓慢。在60%的病例中,诊断后5 - 10年可观察到进展,然而高达25%的CLL快速进展为急性期白血病。
如今,分子遗传诊断方法,如所谓的荧光原位杂交(FISH)技术,允许快速分析存在的遗传改变,例如在CLL中。CLL的重要预后标志物包括人类基因组特定染色体区域的遗传物质丢失(称为“缺失”),仅限于肿瘤细胞。基于fish结果(图1A),可以将个体患者与他们的特定风险结合起来,以经历快速或缓慢的疾病进展。如果只在13号染色体上出现缺失,CLL的有利病程可以预期,而不良预后与11号染色体(所谓的atm基因)和/或17号染色体(p53基因)的缺失有关(图1A)。换句话说:如果发现不利的预测缺失,CLL患者将接受与具有有利遗传标记的患者不同的治疗。
在最近的一项研究中,我们可以证明在培养细胞中比在天然细胞中更好地检测到这种与预后相关的缺失。在CLL特异性培养基中培养4天的细胞中,检出率高出8%以上(图1B)。这是令人惊讶的,因为研究本地材料总是比研究培养出来的材料好,这是常识。背后的想法是,更接近病人的自然状态。这里CLL已被证明是这一规则的例外,因为显然应用的细胞培养条件非常适合恶性CLL细胞的生长和后期检测。为了更好地照顾病人,诊断方案可能应该调整,FISH研究应该在培养细胞中进行,而不是在天然细胞中进行。
托马斯Liehr
耶拿大学医院,弗里德里希·席勒大学,人类遗传学研究所,
德国耶拿大学10号,D-07743
出版
培养细胞中慢性淋巴细胞白血病特异性异常的间期分子细胞遗传学检出率高于血液或骨髓涂片。
Alhourani E, Aroutiounian R, Harutyunyan T, Glaser A, Schlie C, poole B, Liehr T
J组织化学,细胞化学,2016年8月











留言回复
你一定是登录发表评论。