消化对载大分子纳米乳通过肠上皮运输的影响
大分子量亲水性药物的口服给药途径作为最方便的给药途径已被广泛探索。由于多肽和蛋白质等大分子的亲水性、大分子尺寸和易酶降解,口服递送一直是一项挑战。脂质给药系统通过保护大分子不受酶降解和提高肠道上皮的通透性,在提高大分子的口服生物利用度方面显示出巨大的潜力。在以脂质为基础的药物输送系统中,自乳化纳米乳(SEN)具有长期稳定性和易于制备的特点。SEN是脂质和表面活性剂的各向同性混合物,在水中稀释后会自发形成水包油纳米乳。通过SEN提高大分子口服生物利用度的机制之一是通过肠上皮吸收完整的大分子载脂纳米液滴。
脂质纳米液滴体积小,具有脂质性质,可被完整吸收。然而,与装载SEN的大分子通过肠上皮的体外运输相比,装载SEN的大分子的体内口服生物利用度要低。体内增强效果不如体外增强,可能是由于脂质纳米滴的消化作用,导致脂质纳米滴在吸收前释放大分子。脂质纳米滴的大分子释放到外部水相可能会限制大分子的膜渗透,并且由于肠腔的恶劣环境也会导致大分子的广泛降解。
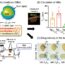
我们的研究目的是研究装载SEN的大分子的消官方manbetx手机版化对大分子通过MDCK上皮细胞单层和离体大鼠肠道运输的影响。以葡聚糖10 kDa为模型大分子。通过形成葡聚糖-磷脂固体分散体,负载于SEN的脂相,制备葡聚糖负载的SEN,并采用体外消化模型模拟体内肠腔。通过体外消化前后葡聚糖负载的SEN的液滴大小和包封效率进行表征。体外消化后,脂质纳米液滴中葡聚糖向外水相的渗漏量增加,葡聚糖负载SEN的液滴尺寸显著增加。将负载葡聚糖的SEN与消化的葡聚糖负载SEN进行比较,由于脂质纳米滴的破坏和葡聚糖释放到SEN的外水相,负载葡聚糖的SEN通过体外MDCK细胞单层的转运减少3.5倍,通过离体大鼠肠道的转运减少1.3 ~ 2.0倍。脂质纳米滴通过肠上皮的转运可以作为无创递送的潜在机制之一进一步探讨大分子。
Pulkit Khatri1,小君邵2
1AmbioPharm, Inc, 1024 Dittman Court, North Augusta, SC 29842, USA
2北京大学药学与健康科学学院药学系,
美国纽约皇后区乌托邦公园路8000号圣约翰大学
出版
消化对葡聚糖负载的自乳化纳米乳通过MDCK上皮细胞单层和大鼠肠道运输的影响。
Khatri P, Shao J
国际医药杂志2018年1月30日










留言回复
你一定是登录发表评论。